Ligacoes Quimicas Teoria Do Octeto Ligacao Ionica Ligacao Metalica

Ligações Químicas Teoria Do Octeto Ligação Iônica Ligação Metálica Portanto, a teoria ou regra do octeto explica a ocorrência das ligações químicas da seguinte forma: “muitos átomos apresentam estabilidade eletrônica quando possuem 8 elétrons na camada de valência (camada eletrônica mais externa).”. 1) o documento discute as principais teorias de ligação química, incluindo a teoria do octeto, ligações iônicas, covalentes e metálicas. 2) a teoria do octeto estabelece que os átomos buscam completar sua camada de valência com oito elétrons para alcançar estabilidade.

3 Ligacoes Quimicas E Geometria Molecular Pdf Ligação Química Por meio das ligações químicas, a maioria dos átomos adquire estabilidade, pois ficam com o seu dueto ou octeto completo, assemelhando se aos gases nobres. Átomos de um elemento com número atômico 20 ao fazer uma ligação iônica devem, no total:. Há três tipos de ligações químicas: ligação iônica – perda ou ganho de elétrons ligação covalente – compartilhamento de elétrons (normal ou dativa) ligação metálica – átomos neutros e cátions mergulhados numa "nuvem eletrônica" ou "mar de elétrons". 1.0 – introdução (regra do octeto) os átomos ligam se para adquirir maior estabilidade. verifica se na natureza, que a grande maioria dos elementos químicos, encontram se ligados a outros, e que somente os gases nobres estão no estado atômico isolados. Conheça as formas de ligação entre os átomos: iônica, covalente e metálica. entenda por que elas ocorrem e também confira exercícios sobre o assunto.
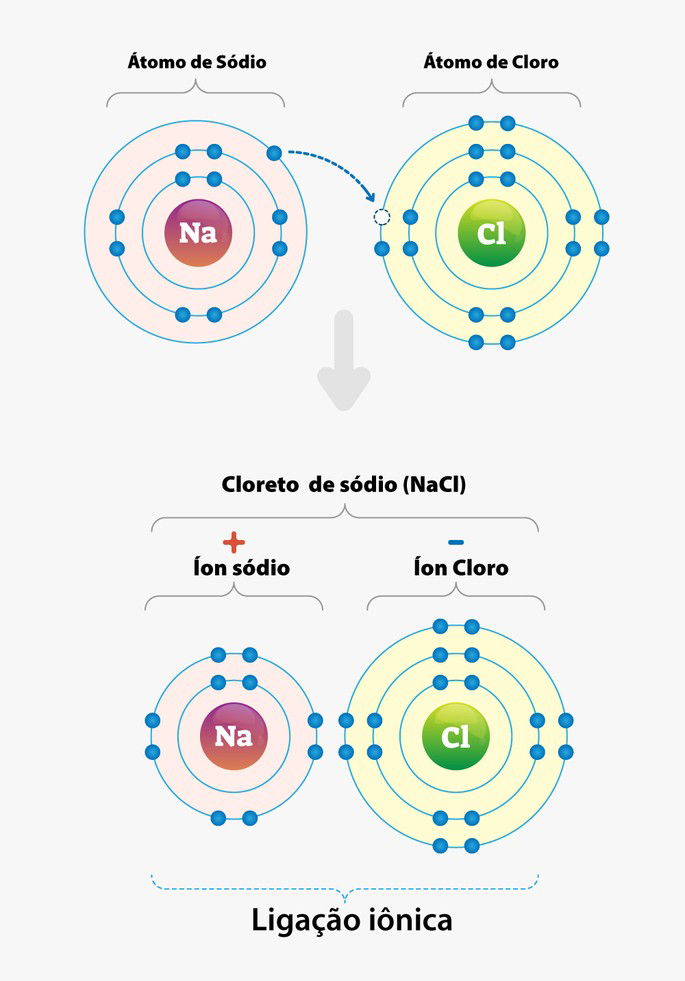
Exemplo De Ligacao Ionica 1.0 – introdução (regra do octeto) os átomos ligam se para adquirir maior estabilidade. verifica se na natureza, que a grande maioria dos elementos químicos, encontram se ligados a outros, e que somente os gases nobres estão no estado atômico isolados. Conheça as formas de ligação entre os átomos: iônica, covalente e metálica. entenda por que elas ocorrem e também confira exercícios sobre o assunto. Os três tipos mais comuns de ligações químicas, consideradas fortes e que estão presentes na maioria das moléculas (ligação iônica, ligação covalente e ligação metálica), são discutidas em detalhe. Representar, com base na regra do octeto, as fórmulas de estrutura de lewis de algumas moléculas, interpretando a ocorrência de ligações covalentes simples, duplas ou triplas. Em materiais com este tipo de ligação, os elétrons se movem livremente (“mar de elétrons”) pelos átomos de metal da estrutura. este é o motivo da alta condutividade dos metais e da sua aplicabilidade em circuitos elétricos. Conheça mais sobre as ligações químicas. veja quais são seus tipos, e observe exemplos de compostos bem como as regras para estabilidade de um átomo.
Química 131 1 Ano Rembrandt Coc Bauru Resumo Regra Do Octeto E Os três tipos mais comuns de ligações químicas, consideradas fortes e que estão presentes na maioria das moléculas (ligação iônica, ligação covalente e ligação metálica), são discutidas em detalhe. Representar, com base na regra do octeto, as fórmulas de estrutura de lewis de algumas moléculas, interpretando a ocorrência de ligações covalentes simples, duplas ou triplas. Em materiais com este tipo de ligação, os elétrons se movem livremente (“mar de elétrons”) pelos átomos de metal da estrutura. este é o motivo da alta condutividade dos metais e da sua aplicabilidade em circuitos elétricos. Conheça mais sobre as ligações químicas. veja quais são seus tipos, e observe exemplos de compostos bem como as regras para estabilidade de um átomo.

Educa Trilha Prof João Batista Ligações Químicas Ligação Iônica Em materiais com este tipo de ligação, os elétrons se movem livremente (“mar de elétrons”) pelos átomos de metal da estrutura. este é o motivo da alta condutividade dos metais e da sua aplicabilidade em circuitos elétricos. Conheça mais sobre as ligações químicas. veja quais são seus tipos, e observe exemplos de compostos bem como as regras para estabilidade de um átomo.
Comments are closed.